PINTREE試験(レムデシビルOPAT)のRCTをまとめました。
前回モルヌピラビルRCTの記事でNNTを比較しましたが、こちらを読み込んでみたらイベント数が少なすぎて(集団が違いすぎて)、単純比較したのはまずかったかなと思ってしまいました。
それにしてもレムデシビルはRCTをやるたびに結果が変わる不思議な薬ですね。モルヌピラビルとレムデシビルは使い分けに困るので、ぜひRCTで勝負をつけていただきたいところです・・・
Early Remdesivir to Prevent Progression to Severe Covid-19 in Outpatients
N Engl J Med. December 22, 2021
DOI: 10.1056/NEJMoa2116846
- Design: Double-blind RCT
- P: 12才以上、発症7日以内で重症化危険因子1つ以上または60才以上の入院していないCOVID-19
- 危険因子:高血圧、心血管・脳血管疾患、DM、BMI≥30、免疫抑制者、CKD、慢性肝疾患、慢性肺疾患、現在の癌、鎌状赤血球症
- 除外基準:過去のCOVID-19入院歴・治療歴、ワクチン接種者、Bw<48kgかつCcr<30、授乳婦
- I: レムデシビル点滴静注 3日間(day1: 200mg, day2, 3: 100mg)
- C: プラセボ 1:1
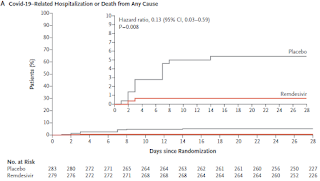
- O: day29におけるCOVID-19による入院、またはあらゆる原因による死亡
結果:
- 各群に292名ずつ割り付けられ、レムデシビル群の13名、プラセボ群の9名が投与を受けなかった
- 平均年齢は50才で、危険因子は肥満55.2%、60歳以上30.2%、DM 61.6%が含まれた
- バリアントは記載ないですが、米国における2020年9月18日~2021年4月8日の試験のため、前半はアルファ株、後半はデルタ株が主流と思われます
- day29の入院または死亡のハザード比は0.13 (95%CI: 0.03-0.59)
- グラフ目視上ARR 5%くらいなので、NNT=20
- 死亡は両群ともday29までには発生しなかった
- 両群の鼻咽頭ウイルス量に明らかな差は認められなかった
- 頻度の高い有害事象は、嘔気(10.8% vs 7.4%)、頭痛(5.7% vs 6.0%) などで、試験レジメンに関連する有害事象はレムデシビル群に多かった(12.2% vs 8.8%)
補足:
- プラセボ群の入院率や死亡率を見る限り、モルヌピラビルやソトロビマブのRCTよりもかなり低リスク者が集められています
- ウィルス量に差がないにも関わらず、臨床症状と入院率が下がるという点が不可解で、解釈に困ります
- 本文中のDiscussionでは、アカゲザルのレムデシビル治療でも上気道ウィルス量と臨床的有効性の乖離があり、下気道ウィルスの減少で説明できるのではないか、とありました
- COVID-19による入院、といういつもと少し違うエンドポイントが採用されていますが、全ての原因による入院or死亡も一応有意差はあります(HR 0.28, 95%CI: 0.10-0.75)